論文紹介LUCUBRATIONS
「誌上ディベート」DHEA補充 Yes vs. No ーYesの立場から

アンチ・エイジング医学18(4):036(284)-041(289), 2022.
はじめに
今回、「誌上ディベート:DHEA補充」に「Yes」の立場での原稿執筆依頼があった。臨床医としてアンチエイジング医療に従事して約15年経つが、この間、DHEA補充療法も実践してきた。その意味で「DHEA補充はYes」という立場になる。本稿では、現場の経験も交えて執筆したい。
DHEAの代謝経路
図1に示すように、デヒドロエピアンドロステロン(dehydroepiandrosterone;DHEA)は、主に副腎でコレステロールから合成され、精巣、卵巣などの末梢組織でテストステロンやエストロゲンに変換される1)。DHEAはこれらのホルモンの上流にあるため、マザーホルモン(mother hormone)とも呼ばれ、またヒトにおいて最も豊富に存在するホルモンである。
図1.ステロイドの代謝経路
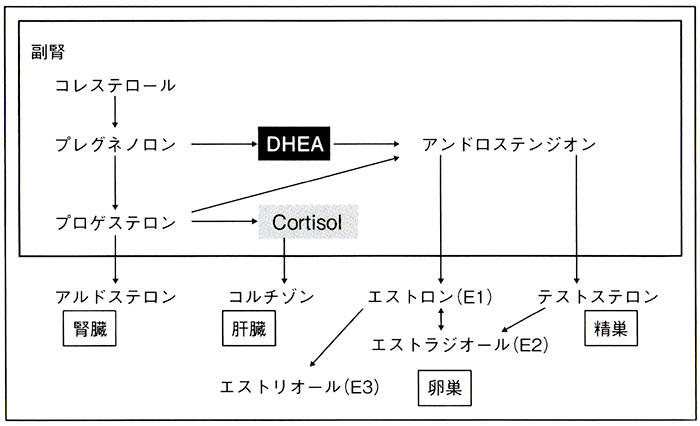 コレステロールからプレグネノロンを経てDHEAが作られる。DHEAはアンドロステンジオンを経てテストステロン、さらにエストラジオールへと変換される。しかし、過剰なストレスがかかると、プレグネノロン→DHEAの経路は遮断され、プレグネノロンからストレスホルモンのコルチゾールが優先的に作られる。(文献1より改変引用)
コレステロールからプレグネノロンを経てDHEAが作られる。DHEAはアンドロステンジオンを経てテストステロン、さらにエストラジオールへと変換される。しかし、過剰なストレスがかかると、プレグネノロン→DHEAの経路は遮断され、プレグネノロンからストレスホルモンのコルチゾールが優先的に作られる。(文献1より改変引用)
アンドロゲンは男性ホルモン作用を有するホルモンの総称で、DHEA、アンドロステンジオン、テストステロンなどを指す。また、DHEAもテストステロンの10分の1程度の弱い男性ホルモン作用を有する。エストロゲンは女性ホルモン作用をもつホルモンの総称で、エストロン、エストラジオール、エストリオールなどを指し、ヒトではエストラジオールが最も活性が高い。
女性の卵巣ではエストロゲン、プロゲステロンの他に、DHEAとテストステロンも産生されている。閉経後は卵巣からのエストロゲン、プロゲステロン、DHEAの産生はなくなり、閉経後のエストロゲン供給の90%は副腎のDHEAに由来する。テストステロンは脂肪組織などに存在するアロマターゼによりエストラジオールに変換される。一方、閉経後も卵巣からのテストステロン分泌はかなり長い間続くことが知られているが、それでもテストステロンの40〜75%は副腎のDHEA由来である2)、3)。
生体内ではDHEAは硫酸化体のDHEA-sulfate(DHEA-S)として99%が存在し、相互に変換される。体内のDHEAを正確に知るためには、血清DHEA-Sを測定する。
DHEAの作用は、変換されたテストステロンやエストロゲンによるものと考えられる一方、DHEA固有の作用もあると考えられている。しかしDHEA固有の受容体の存在も含め、未だ一致した見解には至っていない。
DHEA-S/コルチゾール比
図11)の上流に、プレグネノロン(pregnenolone)とDHEAがあるが、これらを補充すると、下流まで行ってテストステロンやエストラジオールの補充につながるとは必ずしもいえない。
同じ副腎から産生されるステロイドホルモンのコルチゾール(cortisol)は、一生を通じてほとんど変動しない。しかし、過剰なストレスがかかると、ストレスに打ち勝つためにプレグネノロンから優先的にコルチゾールが産生され、血中コルチゾール濃度は上昇し、一方ではプレグネノロンからDHEAに至るルートは遮断され、DHEA、テストステロン、エストロゲンなどの産生が減少する1)。
コルチゾールとDHEAは拮抗的に働く。コルチゾールが過剰になると、血圧や血糖が上昇し、抗炎症作用と同時に免疫機能の低下をまねく。一方、DHEAはストレス抵抗性、免疫機能の維持、骨密度の維持、インスリン抵抗性の改善などに働く。したがって、DHEA-S/コルチゾール比(計算には同一単位を用いる)は、アンチエイジングドックでは重要な指標で必ず測定するが、20以上を目標値としている。
加齢とともに血清DHEA-Sは減少
図2に示すように4)、DHEAは20歳前後をピークに達し、その後直線的に減少する。当院のアンチエイジングドックを受診する50歳以降の受診者のほとんどで血清DHEA-Sは低く、DHEA-S/コルチゾール比では10以下のことが多い。
図2. 加齢に伴う血清DHEA-S濃度の変化
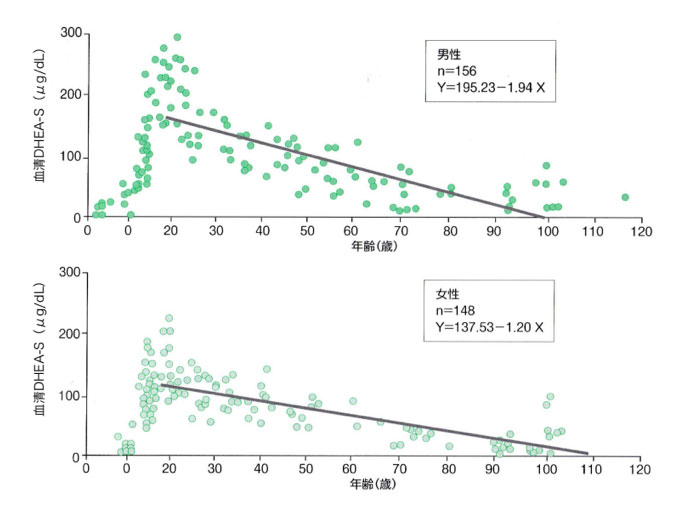 DHEA-Sは20歳前後でピークとなり、その後は加齢に伴って急速に低下する。(文献4より改変引用)
DHEA-Sは20歳前後でピークとなり、その後は加齢に伴って急速に低下する。(文献4より改変引用)
DHEAの低下が高度の場合、腋毛、恥毛の脱落として気づかれることもある。これは女性の腋毛、恥毛の発育が100%DHEAに依存しているからである。軽度の場合には、性欲の低下程度であり、自他覚的に気付かれにくい。5)。
DHEA補充療法についての研究
先に図2で示したように、DHEAは加齢に伴い減少する。多くの疾患の発症率が高まる頃には、DHEAはかなり低い濃度になることから、老化を遅らせたり、廊下を予防したりすることに関係するホルモンと考えられてきた。1980年代からDHEA補充の考え方が広まり、投与がはじまった6)。
初期のDHEA研究の主な成果として、性機能、健康感(well-being)、代謝パラメータ、免疫反応、認知機能などの改善が示唆された。しかし、これらの初期研究は、副腎からDHEAを分泌しないラットやマウスの実験で得られた成績であった。その後、これらの効果の実証がヒトで試みられたが、一致した結果が得られないこともあった。その理由に、実験に用いた動物とヒトの違いをあげる研究者もいる7)。
DHEA低値が、認知障害、免疫機能障害、一部のがん、炎症性疾患、2型糖尿病、心血管障害などと、関連するとの複数の臨床報告がある。
一方DHEAの、免疫賦活作用、抗骨粗鬆症作用、抗肥満作用、抗腫瘍作用、抗動脈硬化作用、抗糖尿病作用、中枢神経系への作用(気分や健康感の改善、認知機能の向上)、なども報告されている。
疫学調査でも、DHEAは早くから長寿に関係するホルモンとして注目されてきた。例えばボルチモア長期縦断研究では、DHEA-Sが高値は長寿であることが示されている8)。また、福岡県田主丸町住民検診の27年間の追跡研究でもDHEA-Sは男性の長寿の予測因子と報告されている9)。このことからDHEAは長寿ホルモンとも呼ばれることもある。
DHEA補充療法の効果を証明する臨床研究は、それほど多くはなく、また小規模であるために、基礎研究で期待されるような効果を高いエビデンスレベルで証明するまでには至っていない。
DHEA補充療法の副作用
女性におけるテストステロンの過剰は、ざ瘡(ニキビ)、多毛症、生理不順(無月経)、頭頂部脱毛、声の低音化、体型の男性化などを引き起こす6)。DHEAの副作用として、50mg/日以上の用量では、ニキビ、顔の毛の成長=多毛症、脂性肌(皮膚が脂ぎる)などのアンドロゲン作用によるものが報告されているが10)11)、重大な有害事象の報告はない。
思春期のざ瘡(ニキビ)は、その時期のDHEAの生理的上昇と関連している。DHEAはヒト皮脂腺においてDHT(dihydrotestosterone)に変換され、ざ瘡(ニキビ)の原因となる6)。
ポーランドの更年期医学会専門家会議の見解
2020年のポーランド男性女性更年期医学会専門家会議(expert panel of Polish Menopause and Andropause Society)は、「-閉経前及び閉経後のDHEA補充について-の見解(position statement)」を公表した12)。その要旨は以下のとおりである。
2020年の時点で報告されている臨床試験やメタアナリシスの論文をレビューし、DHEA補充療法は以下の状態に有効であることを示している。
(1)副腎機能不全を有する女性、(2)副腎皮質ステロイドホルモン剤によって慢性的に治療を受けている女性、(3)低骨密度や骨粗鬆症の閉経後女性、(4)性機能障害や性欲減退に悩む閉経前の女性、(5)閉経や泌尿生殖器症候群による外陰膣の萎縮に悩む女性、などである。
また、最近の臨床試験によってDHEA補充療法がおそらく効果的である状態として以下をあげている。
(1)性機能障害や性欲減退に悩む閉経後女性、(2)卵巣予備能の低下した不妊女性、(3)うつや不安に悩む女性、(4)肥満やインスリン抵抗性を有する女性などである。
そして重要な点として、今までの臨床試験において重篤な副作用の報告が1つもみられないことを強調している。
ポーランド更年期医学会が、閉経前および閉経後の女性に対するDHEA補充療法の対象とした上記の状態は、現時点では多くの専門家のコンセンサスが得られるものと筆者は考えている。次項に上記のいくつかの状態ついて説明する。
卵巣予備能の低下した不妊女性に対するDHEA補充療法
日本も晩婚化とともに、高齢で妊娠を希望する女性も多くなってきている。40歳代で出産する女性も増加しており、これには生殖補助医療(ART)の進歩が関係している。ARTとは、排卵誘発剤で卵巣を刺激して卵胞を発育させる。卵巣から取り出した卵子を体外で精子と受精させ子宮に戻す体外受精が一般的である。
不妊女性に4〜5ヵ月間DHEAを補充すると、血中AMH(anti-mullerian hormone)量、排卵数、胚の質、妊娠率が有意に増加することが報告されている。血中AMHは、簡単に言えば「卵巣年齢の推定」検査で、この値が高ければ、妊娠・出産のチャンスが高いといえる。
2015年コクランは、体外受精を受ける女性に対するDHEA補充の効果をレビューした。(コクランとは、エビデンスに基づき医学論文のシステマティック・レビューを行う国際的団体で、その水準の高さから医療関係者が常に参考にする)13)。その結果、プラセボ群で生児出産/妊娠継続率が12%であったのに対し、DHEA補充群では、15~26%に増加し、妊娠の割合が高かったと報告された。しかし、結論を出すにはまだエビデンスが不十分であり、安全性についても今後の研究を待たなければならないとしている。
DHEA補充は日本のARTの現場でも試みられているようで、不妊女性の福音になることが期待される。
DHEA補充療法と認知機能
DHEA補充による認知機能や健康感(well-being)の改善については、未だ議論がある。
2000年のコクランでは、健康感の改善については限定的ながら認めたが、認知機能の改善については否定的だとした14)。2006年コクランは、再度高齢者の記憶力や認知機能に対するDHEA補充の改善効果について過去の論文をレビューした。その結果、それを裏付けるエビデンスは目下のところはなく、さらに質の高い臨床試験が必要だと報告している15)。
本邦においてヒトに対するDHEA補充療法についての報告は少ない。秋下は、軽度の認知機能障害のある女性にDHEA25mg/日を処方し,6ヵ月間経過をみたところ,単語記憶,遅延再生などの認知機能が改善されたと報告している16)。
DHEA補充による認知機能の改善効果については、さらなる研究が必要のようである。
DHEA補充療法と骨粗鬆症
Jankowskiらは、DHEA補充が骨粗鬆症の治療や予防に役立つ可能性を報告している17)。テストステロンとプロゲステロンは骨形成を促進し、エストロゲンは骨吸収を抑制するが、DHEAもエストロゲンと同様に、骨吸収を抑制する可能性がある。さらに、DHEAはテストステロンと同様に弱いアンドロゲンであるため、骨形成にも関与している可能性がある。したがって、DHEAは、骨形成を促進し骨吸収を抑制することで、骨粗鬆症を予防すると考えられる。
閉経後の性機能低下に対するDHEA補充療法
閉経後は膣上皮の萎縮が進むため分泌物も少なくなり性交痛の原因となる。このことは性機能(性交回数、性的満足度、性欲など)の低下につながる。
DHEA補充療法は、膣上皮を改善して分泌物の量も多くし、性交痛を和らげ、性機能が改善した12)。膣上皮の改善はDHEAから変換されたエストロゲンの効果、性機能の改善はDHEAから変換されたテストステロンの効果と筆者は考えている。ホルモン補充療法(HRT)だけでは性機能の改善が得れないこともあり、その時はDHEA補充を追加することもある。
当院でのDHEA補充療法の経験
当院では、DHEA-S低値(DHEA-S/コルチゾール比が20以下)の患者に健康感増進を目的に、DHEA補充療法を勧めている。その内の10人(男4人、女6人)は3年以上(3〜9年、平均6年)、DHEA補充療法(25mg/日服用)を続けている。図3にDHEA補充前後の血清DHEA-S濃度を示す。
図3. DHEA-S値(10名)(DHEA補充療法前後)
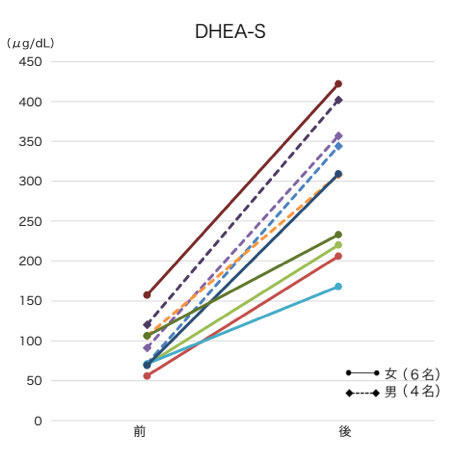 DHEA補充療法前後の血清DHEA-S濃度を示す。DHEA服用前のDHEA-Sは平均で92μg/dL、後は297μg/dLである。(筆者作成)
DHEA補充療法前後の血清DHEA-S濃度を示す。DHEA服用前のDHEA-Sは平均で92μg/dL、後は297μg/dLである。(筆者作成)
図4. DHEA補充療法(10名)(抗加齢QOL共通問診票)
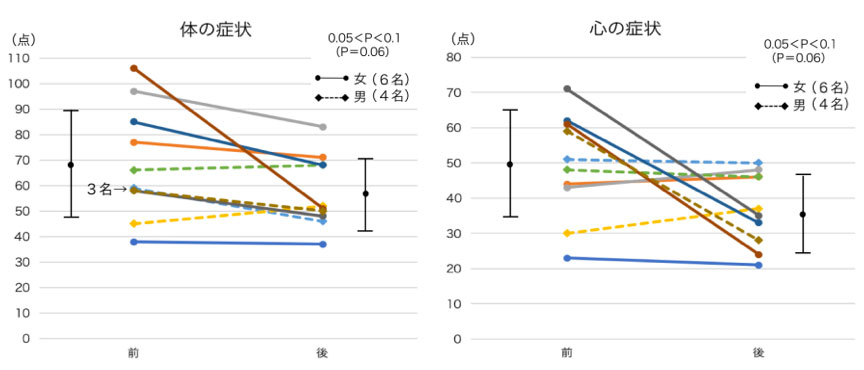 抗加齢QOL共通問診票でDHEA補充前後での症状の改善度をみた。左は体の症状、右は心の症状であるが、ともに有意差はないが、改善の傾向を認める(筆者作成)
抗加齢QOL共通問診票でDHEA補充前後での症状の改善度をみた。左は体の症状、右は心の症状であるが、ともに有意差はないが、改善の傾向を認める(筆者作成)
図5. DHEA補充療法前後の総テストステロン(TT)値(女性6名)
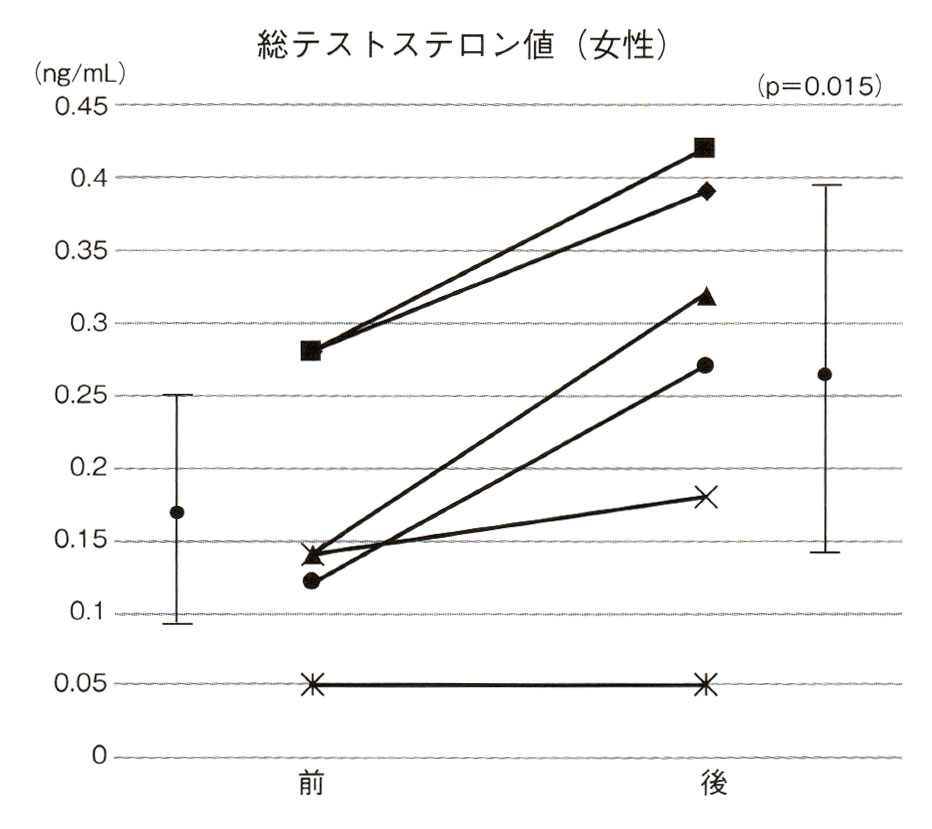 DHEA25mg/日の補充療法により、TT値は前の0.168±0.084から後の0.272±0.126ng/Lへと有意に増加した(P=0.015)。補充後のTT値は、服用3〜9年(平均5.9年)の値である。筆者作成)
DHEA25mg/日の補充療法により、TT値は前の0.168±0.084から後の0.272±0.126ng/Lへと有意に増加した(P=0.015)。補充後のTT値は、服用3〜9年(平均5.9年)の値である。筆者作成)
DHEA補充療法中は、3ヵ月に一度、血清DHEA-S濃度を測定し、25〜30歳時の生理的範囲に収まるように、用量調整を行なっている。
おわりに
米国のスーパーなどでは、DHEAはサプリメントとして売られている。しかし、日本をはじめ多くの国では医薬品として取り扱わなければならない。使われている用法・用量も異なるので、安全に使用するためには、血清DHEA-S測定を定期的に行い、生理的範囲にあることを確かめながら、医師が処方することが必要である。
日本の医療費の増大は待ったなしの状況である。発病してから治療するのではなく、病気にならないために未病の段階での予防医療が必要である。その有効な手段の1つに、DHEA補充をはじめとするホルモン補充療法があると筆者は考えている。
最後に、2021年DHEAがインターロイキン6(IL-6)を特異的に抑制することで、新型コロナ感染症(COVID-19)を緩和する可能性が報告されていることを付け加えておきたい18)。
文献
- 色本涼, 三村將. 心身ストレスの検査と評価. In: 日本抗加齢医学会専門医・指導士認定委員会. アンチエイジング医学の基礎と臨床(第3版). 東京:株式会社メジカルビュー社; 2015. 189-190.
- Klinge CM, Clark BJ, Prough RA. Dehydroepiandrosterone Research: Past,Current,and Future. Vitam Horm. 2018:108:1–28.
- Longcope C. Adrenal and gonadal androgen secretion in normal females. Clin Endocrinol Metab. 1986:15(2):213–28.
- 柳瀬敏彦. 副腎ホルモン. In: 日本抗加齢医学会専門医・指導士認定委員会. アンチエイジング医学の基礎と臨床(第3版). 東京:株式会社メジカルビュー社; 2015:108-109.
- 柳瀬敏彦. 女性におけるテストステロンの意義. 日本女性医学誌. 2020;27:548-551.
- Rutkowski K, Sowa P, Rutkowska-Talipska J, et al. Dehydroepiandrosterone (DHEA): hypes and hopes. Drugs. 2014:74(11):1195-207.
- Davis SR, Panjari M, Stanczyk FZ. DHEA Replacement for Postmenopausal Women. J Clin Endocrinol Metab. 2011;96(6):1642–53.
- Roth GS, Lane MA, Ingram DK, et al. Biomarkers of caloric restriction may predict longevity in humans. Science. 2002; 297(5582): 811.
- Enomoto M, Adachi H, Fukami A, et al. Serum dehydroepiandrosterone sulfate levels predict longevity in men: 27-year follow-up study in a community-based cohort (Tanushimaru study). J Am Geriatr Soc. 2008; 56:994-8.
- Kroboth P, Salek F, Pittenger A, et al. DHEA and DHEA-S: a review. J Clin Pharmacol. 1999; 39(4):327-48.
- Panjari M, Davis S. DHEA for postmenopausal women: a review of the evidence. Maturitas. 2010; 66(2):172-9.
- Rabijewski M, Papierska L, Binkowska M, et al. Supplementation of dehydroepiandrosterone (DHEA) in pre- and postmenopausal women – position statement of expert panel of Polish Menopause and Andropause Society. Ginekologia Pol. 2020; 91(9), 554–562.
- Nagels HE, Rishworth JR, Siristatidis CS, et al. Androgens (dehydroepiandrosterone or testosterone) for women undergoing assisted reproduction. Cochrane Database Syst Rev. 2015; 11:CD009749.
- Huppert FA ,Van Niekerk JK, Herbert J. Dehydroepiandrosterone (DHEA) supplementation for cognition and well-being. Cochrane Database Syst Rev. 2000; 2:CD000304.
- Grimley Evans J, Malouf R, Huppert FAH, et al. Dehydroepiandrosterone (DHEA) supplementation for cognitive function in healthy elderly people. Cochrane Database of Systematic Reviews. 2006; 2006: CD006221.
- 秋下雅弘. ホルモン補充療法の将来性. 日老医誌. 2009; 46:327-32s9.
- Jankowski CM , Gozansky WS, Schwartz RS, et al. Effects of dehydroepiandrosterone replacement therapy on bone mineral density in older adults: a randomized, controlled trial. J Clin Endocrinol Metab. 2006; 91(8):2986-93.
- Tomo S, Banerjee M, Sharma P, et al. Does dehydroepiandrosterone sulfate have a role in COVID-19 prognosis and treatment? Endocr Regul. 2021; 55(3):174-181.



